Por favor, avalie esta postagem
A COVID-19 grave causa trombose capilar pulmonar precoce, levando a desconforto respiratório, com estudos enfatizando o tratamento anticoagulante imediato para mitigar complicações.
Cientistas da Universidade de São Paulo descobriram que o COVID-19 grave é causado principalmente por danos aos pequenos vasos sanguíneos dos pulmões, resultado da infecção por SARS-CoV-2.
A formação de coágulos sanguíneos (trombose) nos pequenos vasos sanguíneos dos pulmões é um resultado precoce de doença grave. COVID 19muitas vezes ocorrendo antes das dificuldades respiratórias causadas por danos generalizados aos sacos aéreos, de acordo com um estudo brasileiro relatado em artigo publicado no Jornal de Fisiologia Aplicada. Os exames post-mortem de nove indivíduos que faleceram de COVID-19 grave revelaram um padrão distinto de alterações na estrutura dos vasos sanguíneos pulmonares e trombose.
Pela primeira vez, o artigo descreve aspectos subcelulares do dano endotelial e fenômenos trombóticos associados causados pela infecção. Observa o impacto da inflamação aguda na circulação microvascular pulmonar como o fator chave na COVID-19 grave, contribuindo para uma compreensão mais profunda da fisiopatologia da doença e para o desenvolvimento de novas estratégias terapêuticas.
“Este estudo forneceu a prova final do que vínhamos apontando desde o início da pandemia – que a COVID-19 grave é uma doença trombótica. O vírus SARS-CoV-2 tem um tropismo para (é atraído por) o endotélio, a camada de células que reveste os vasos sanguíneos. Quando invade as células endoteliais, afeta primeiro a circulação microvascular. O problema começa nos capilares dos pulmões (os minúsculos vasos sanguíneos que circundam os alvéolos), seguida de coagulação nos vasos maiores que podem atingir qualquer outro órgão”, disse a pneumologista Elnara Negri, primeira autora do artigo e professora da Faculdade de Medicina da Universidade de São Paulo (FM-USP). Ela foi uma das primeiras pesquisadoras do mundo a chegar à conclusão de que a COVID-19 grave é uma doença trombótica.
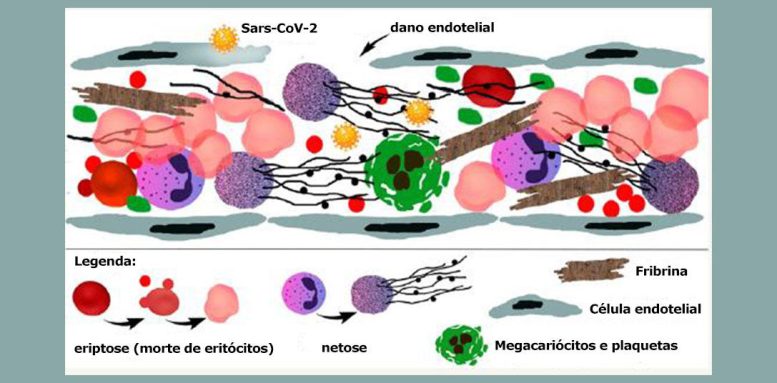
Os pesquisadores da USP analisaram tecido pulmonar de nove pacientes que morreram de COVID-19. Crédito: Elia Caldini
No estudo, apoiado pela FAPESP, os pesquisadores usaram microscopia eletrônica de transmissão e varredura para observar os efeitos do vírus nas células endoteliais pulmonares de pacientes graves de COVID-19 que morreram no Hospital das Clínicas, complexo hospitalar operado pela FM-USP .
Todas as nove amostras obtidas por autópsias minimamente invasivas apresentaram uma alta prevalência de microangiopatia trombótica – coágulos sanguíneos microscópicos em pequenas artérias e capilares que podem causar danos a órgãos e lesões isquêmicas de tecidos. As amostras vieram de pacientes que ficaram internados entre março e maio de 2020, necessitaram de intubação e cuidados intensivos e faleceram por hipoxemia refratária e insuficiência respiratória aguda.
Vale ressaltar que nenhum dos pacientes incluídos no estudo foi tratado com anticoagulantes, pois isso não fazia parte do protocolo de tratamento da COVID-19 na época. Também não havia vacinas contra a COVID-19 disponíveis no período.
Eliminação do glicocálice endotelial
Negri explicou que o próprio endotélio é revestido por uma camada de glicoproteínas semelhante a um gel chamada glicocálix, que atua como uma barreira para regular o acesso de macromoléculas e células sanguíneas à superfície endotelial. Esta barreira evita a coagulação nos vasos sanguíneos, inibindo a interação das plaquetas com o endotélio.
“Estudos anteriores realizados por Helena Nader na UNIFESP (da Universidade Federal de São Paulo) mostraram que o SARS-CoV-2 invade as células principalmente por ligação ao receptor ACE-2 (uma proteína na superfície de vários tipos de células, incluindo células epiteliais e endoteliais do sistema respiratório), mas antes disso, liga-se ao sulfato de heparano (um polissacarídeo), um componente importante do glicocálix nas células endoteliais. Quando invade o endotélio, desencadeia desprendimento e destruição do glicocálice, resultando em exposição tecidual e coagulação intravascular. O processo começa na microcirculação”, explicou Negri.
Como o vírus atua inicialmente na microcirculação pulmonar, os exames de contraste realizados durante a pandemia para investigar a presença de coágulos sanguíneos em vasos maiores em pacientes graves com COVID-19 não conseguiram detectar o problema em nenhum estágio inicial, acrescentou ela. Contudo, a disfunção endotelial é um fenómeno chave na COVID-19, uma vez que está diretamente associada à ativação da resposta inflamatória característica da doença.
“A invasão viral maciça e a destruição do endotélio quebram a barreira endotelial e prejudicam o recrutamento de células imunes circulantes, ativando vias associadas à trombogênese e à inflamação”, disse ela.
No estudo, os pesquisadores descobriram que a lesão endotelial tende a preceder dois processos comuns em casos de dificuldade respiratória: vazamento significativo da membrana alvéolo-capilar e acúmulo intra-alveolar de fibrina (associado à coagulação sanguínea e à cicatrização de feridas).
Um estudo do mesmo grupo da FM-USP, liderado por Thais Mauad e incluindo transcriptômica (análise de todos ARN transcritos, codificantes e não codificadores), mostraram que várias vias associadas à coagulação sanguínea e à ativação plaquetária foram ativadas antes da inflamação nos pulmões de pacientes com danos alveolares.
A análise também confirmou que a coagulação não era típica do processo habitual desencadeado pela ativação de fatores de coagulação. “No COVID-19, a coagulação é devida à lesão endotelial e exacerbada pela NETose (um mecanismo imunológico envolvendo morte celular programada através da formação de armadilhas extracelulares de neutrófilos ou NETs), glóbulos vermelhos dismórficos e ativação plaquetária, o que torna o sangue mais espesso e causa muitas complicações”, disse Negri.
Quando o sangue é espesso e altamente trombogênico, acrescentou ela, o paciente deve ser mantido hidratado, enquanto o dano alveolar difuso nas síndromes de desconforto respiratório agudo devido a outras causas requer hidratação reduzida. “Além disso, o momento e o controlo rigoroso da anticoagulação são fundamentais”, sublinhou.
Outro estudo do mesmo grupo de pesquisadores, incluindo Marisa Dolhnikoff e Elia Caldini, mostrou que danos pulmonares na COVID-19 grave estão associados ao grau de NETose: quanto maior o nível de NETs no tecido pulmonar obtido por autópsia, mais os pulmões foram danificadas.
Negri disse que começou a suspeitar que havia uma ligação entre COVID-19 e trombose no início da pandemia, quando percebeu um fenômeno que lembrava sua experiência há cerca de 30 anos com pacientes que tiveram coagulação microvascular após cirurgia de coração aberto com circulação extracorpórea e oxigenador de bolha. , não é mais utilizado porque causa dano endotelial.
“Era uma técnica muito utilizada há 30 anos, mas causa lesões pulmonares muito semelhantes às observadas na COVID-19. Então eu já tinha visto. Além da lesão pulmonar, outra semelhança é a ocorrência de fenômenos trombóticos periféricos, como dedos vermelhos, por exemplo”, disse.
“À medida que a COVID-19 grave se instala, a queda nos níveis de oxigênio no sangue é secundária à trombose capilar pulmonar. Inicialmente, não há acúmulo de líquido nos pulmões, que não ficam “saturados” e não perdem a complacência ou a elasticidade. Isso significa que os pulmões dos pacientes com COVID-19 grave não se parecem com esponjas cheias de líquido, como acontece na síndrome do desconforto respiratório agudo (ARDS) pacientes. Pelo contrário, a insuficiência respiratória associada à COVID-19 grave envolve desidratação dos pulmões. Os alvéolos ficam cheios de ar, mas o oxigênio não consegue entrar na corrente sanguínea devido à coagulação capilar. Isto leva ao que chamamos de ‘hipóxia feliz’, onde os pacientes não sentem falta de ar e não estão conscientes de que a sua saturação de oxigénio está perigosamente baixa.”
Ao observar a intubação de um paciente grave com COVID-19, Negri percebeu que o tratamento desses casos deveria ser totalmente diferente daquele que era no início da pandemia. “O segredo para tratar pacientes graves com COVID-19 é mantê-los hidratados e usar anticoagulante na dose certa, ou seja, a dose necessária no ambiente hospitalar no início da dessaturação de oxigênio, ou seja, baixos níveis de oxigênio no sangue”, ela disse. “Depois disso, a dose terapêutica do anticoagulante deve ser calculada diariamente com base em exames de sangue, sempre em ambiente hospitalar, para evitar qualquer risco de sangramento. A profilaxia é necessária em média quatro a seis semanas após a alta porque é esse o tempo que o endotélio leva para se regenerar.”
Este protocolo de hidratação e anticoagulação é necessário porque, em contraste com outros tipos de SDRA em que o oxigênio nos pulmões é impedido de entrar na corrente sanguínea principalmente pela inflamação alveolar, o dano endotelial dos capilares pulmonares é o principal obstáculo na COVID-19 grave inicial, ela explicou.
“Ninguém sabia desta diferença entre a COVID-19 e outros tipos de SDRA logo no início da pandemia. Na verdade, é por isso que tantos pacientes italianos morreram em UTIs (unidades de terapia intensiva), por exemplo. O protocolo de tratamento utilizado naquela época era diferente”, lembrou ela.
Em 2020, antes de o estudo ser divulgado no Jornal de Fisiologia Aplicada, Negri e seu grupo já haviam observado que o uso do anticoagulante heparina melhorava a saturação de oxigênio em pacientes críticos. Em 2021, em colaboração com colegas de vários países, conduziram um ensaio clínico randomizado no qual conseguiram demonstrar que o tratamento com heparina reduziu a mortalidade grave por COVID-19. As descobertas foram publicadas no Jornal Médico Britânico.
“Esse estudo ajudou a provocar uma mudança global nas diretrizes de tratamento da COVID-19, mostrando que o risco de mortalidade da COVID-19 caiu 78% quando a anticoagulação foi iniciada em pacientes que precisavam de suplementação de oxigênio, mas ainda não estavam na terapia intensiva”, disse Negri. .
A disfunção endotelial deve ser revertida sem demora na COVID-19 grave, utilizando um anticoagulante, explicou ela. “A coagulação do sangue deve ser interrompida o mais rápido possível para evitar o desenvolvimento de problemas respiratórios agudos e outras consequências da doença, como os problemas agora conhecidos como COVID longo”, disse ela.
Um artigo publicado recentemente em Medicina da Natureza por pesquisadores afiliados a instituições do Reino Unido reforça o caráter trombótico da doença, relatando um estudo em que os únicos marcadores de prognóstico longo de COVID identificados foram o fibrinogênio e o dímero D, proteínas associadas à coagulação.
“O estudo mostra que a COVID longa resulta de trombose tratada inadequadamente. O problema microcirculatório pode persistir em vários órgãos, incluindo cérebro, coração e músculos, como se o paciente estivesse tendo pequenos infartos”, disse Negri.
Referência: “Caracterização ultraestrutural do dano microvascular alveolar na insuficiência respiratória grave por COVID-19” por Elnara Marcia Negri, Marlene Benchimol, Thais Mauad, Amaro Nunes Duarte-Neto, Maiara Gottardi, Luiz Fernando Ferraz da Silva, Paulo Hilario Nascimento Saldiva, Marisa Dolhnikoff , Wanderley de Souza e Elia Garcia Caldini, 1º de outubro de 2023, Jornal de Fisiologia Aplicada.
DOI: 10.1152/japplfisiol.00424.2023
“Perfis agudos de biomarcadores sanguíneos predizem déficits cognitivos 6 e 12 meses após a hospitalização por COVID-19” por Maxime Taquet, Zuzanna Skorniewska, Adam Hampshire, James D. Chalmers, Ling-Pei Ho, Alex Horsley, Michael Marks, Krisnah Poinasamy, Betty Raman, Olivia C. Leavy, Matthew Richardson, Omer Elneima, Hamish JC McAuley, Aarti Shikotra, Amisha Singapuri, Marco Sereno, Ruth M. Saunders, Victoria C. Harris, Linzy Houchen-Wolloff, Neil J. Greening, Parisa Mansoori, Ewen M. Harrison, Annemarie B. Docherty, Nazir I. Lone, Jennifer Quint, Naveed Sattar, Christopher E. Brightling, Louise V. Wain, Rachael E. Evans, John R. Geddes, Paul J. Harrison e PHOSP-COVID Study Collaborative Group, 31 de agosto de 2023, Medicina da Natureza.
DOI: 10.1038/s41591-023-02525-y
O estudo foi financiado pela Fundação de Amparo à Pesquisa do Estado de São Paulo.
