Por favor, avalie esta postagem
Um exemplo de acúmulo de nanopartículas em uma biópsia retirada de um rim humano corado com vasculatura. As nanopartículas com alvo vascular estão em vermelho; controlar partículas não direcionadas estão em verde. (Foto de Jenna DiRito e Gregory T. Tietjen)
Ao combinar o uso de nanopartículas transportadoras de medicamentos com uma máquina de preservação de órgãos, os pesquisadores de Yale desenvolveram um procedimento que poderia ajudar a melhorar os resultados a longo prazo para os receptores de transplantes.
Uma tecnologia conhecida como máquina de perfusão normotérmica ex vivo (NMP) surgiu nos últimos anos como um meio de manter um órgão doador “vivo” fora do corpo antes da implantação. O processo envolve o bombeamento de glóbulos vermelhos quentes e oxigenados através de um órgão removido de um doador falecido. Isso ajuda a reparar danos ao órgão e dá aos médicos tempo para avaliar a qualidade do órgão. Também ajudou a aumentar o número de órgãos adequados para transplante.
Em colaboração com investigadores da Universidade de Cambridge, os investigadores de Yale estão a trabalhar para expandir as capacidades de reabilitação da tecnologia com um sistema de administração de medicamentos baseado em nanopartículas que pode fornecer uma variedade de tratamentos diretamente a alvos críticos num rim humano enquanto ainda está no dispositivo. . Seus resultados foram publicados hoje na Science Translational Medicine.
A equipe de Yale, da Faculdade de Medicina e da Escola de Engenharia e Ciências Aplicadas, concentrou-se especificamente no tratamento das células endoteliais vasculares do órgão. Essas células, que revestem a superfície das células sanguíneas, são o primeiro ponto de contato com o sistema imunológico do receptor após o transplante e são essenciais para a aceitação do órgão pelo corpo. O tratamento direto dessas células com medicamentos que bloqueiam temporariamente a sinalização inflamatória para o sistema imunológico do receptor permite que o enxerto cicatrize e aumenta as chances de sucesso do transplante a longo prazo. Também poderia diminuir a chance de infecção, facilitando a imunossupressão sistêmica após o transplante, disseram os pesquisadores.
As células endoteliais são consideradas um alvo ideal porque são facilmente acessíveis enquanto o órgão está na máquina e porque alterações nessas células alertam o sistema imunológico do hospedeiro de que o órgão é estranho e sobre qualquer dano que o órgão possa ter, disse um dos líderes do projeto. , Jordan Pober, professor de medicina translacional da Bayer e vice-presidente de imunobiologia. Ambos os sinais podem desencadear rejeição.
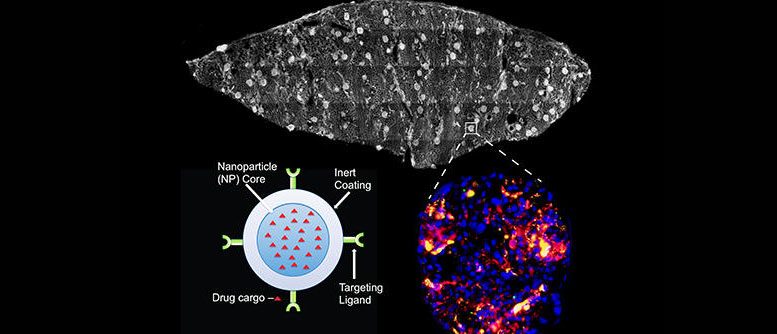
Diagrama da nanopartícula transportadora de fármaco (canto inferior esquerdo); imagem de uma biópsia retirada de um rim humano corado com vasculatura (canto superior direito). A imagem destacada e ampliada é um exemplo de acumulação de nanopartículas. As nanopartículas com alvo vascular estão em vermelho; controlar partículas não direcionadas estão em verde. (Foto de Jenna DiRito e Gregory T. Tietjen)
“Sabemos muito sobre quais são essas alterações no endotélio e como mascará-las para reduzir a rejeição”, disse Pober.
Para atingir as células, os pesquisadores revestiram nanopartículas desenvolvidas no laboratório de Mark Saltzman, professor de Engenharia Biomédica, Engenharia Química e Ambiental e Fisiologia da Fundação Goizueta, com um anticorpo que tem como alvo o CD31, uma proteína abundante no endotélio. Essas partículas, juntamente com um grupo de controle de partículas não-alvo, foram injetadas no dispositivo de perfusão enquanto seu fluido passava por um rim do doador por períodos de quatro a seis horas.
“Para estes estudos, produzimos nanopartículas revestidas de anticorpos a partir de polímeros que são bem conhecidos por serem seguros em humanos, por isso prevemos que esta tecnologia possa ser rapidamente traduzida na prática clínica”, disse Saltzman, outro líder do projeto. Saltzman também é membro do Yale Cancer Center. “Já mostramos anteriormente que essas nanopartículas liberam agentes lentamente ao longo do tempo, de modo que o efeito do tratamento pode durar bem após a conclusão do transplante do órgão.”
Eles descobriram que, em média, o acúmulo de partículas-alvo ao redor das células endoteliais poderia atingir de duas a cinco vezes maior do que no grupo de controle. Em certas regiões de alguns dos rins mais bem perfundidos, porém, as acumulações foram muito mais elevadas, com níveis superiores a 10 vezes os das partículas de controlo.
Os pesquisadores acompanharam os acúmulos usando uma abordagem baseada em microscopia quantitativa de duas cores. As partículas direcionadas a CD31 foram carregadas com corante fluorescente vermelho e as partículas de controle foram carregadas com corante verde. Com a configuração da microscopia, a proporção do sinal vermelho para verde era um indicador confiável das intensidades das duas partículas.
Além de atingir com sucesso as células endoteliais vasculares, a pesquisa representa outro avanço: o desenvolvimento de uma plataforma para estudar esses sistemas de administração de medicamentos em órgãos humanos.
“Já é muito difícil obter partículas onde elas são necessárias após a entrega sistêmica, e mesmo que isso seja possível em um animal, é muito provável que as condições sejam diferentes em uma pessoa”, disse Gregory Tietjen, professor assistente de cirurgia e primeiro autor. do papel. Tietjen, que abriu um novo laboratório focado no uso da plataforma de perfusão ex vivo para desenvolver nanomedicamentos mais precisos, disse estar “animado por ter esta infraestrutura que desenvolvemos para fazer este tipo de trabalho pré-clínico e quantitativo em órgãos humanos”.
“Acreditamos que pode não apenas fornecer novas estratégias terapêuticas para transplante de órgãos, mas também tem o potencial de fornecer novos insights para a administração sistêmica de medicamentos”.
Referência: “Nanopartículas direcionadas ao endotélio durante a perfusão normotérmica de rins humanos” por Gregory T. Tietjen, Sarah A. Hosgood, Jenna Dirito, Jiajia Cui, Deeksha Deep, Eric Song, Jan R. Kraehling, Alexandra S. Piotrowski-Daspit , Nancy C. Kirkiles-Smith, Rafia Al-Lamki, Sathia Thiru, J. Andrew Bradley, Kourosh Saeb-Parsy, John R. Bradley, Michael L. Nicholson, W. Mark Saltzman e Jordan S. Pober, 29 de novembro de 2017, Medicina Translacional Científica.
DOI: 10.1126/scitranslmed.aam6764
